| | | L'électrolyse, mais c'est très simple... |  |
| | | Auteur | Message |
|---|
Asl
Support Electronique
Membre d'Honneur


Age : 73
Localisation : Près de Saumur
Prénom : Alain
Date d'inscription : 15/08/2006
 |  Sujet: L'électrolyse, mais c'est très simple... Sujet: L'électrolyse, mais c'est très simple...  Mer 3 Déc 2008 - 21:09 Mer 3 Déc 2008 - 21:09 | |
| Bonjour, Je reste persuadé que si nous analysons correctement ce qui se passe réellement dans une électrolyse classique, nous pourrons probablement obtenir les clés de notre réussite.Donc, notre petit atome d'hydrogène : Rencontre de deux atomes d'hydrogène, donne une molécule d'hydrogène (H2) : Et la rencontre de deux atomes d'hydrogène avec un atome d'oxygène donne une molécule d'eau : Jusque là, aucun scoop. Passons maintenant à l'électrolyse et détaillons le plus précisément (???) possible les réactions :Un sel (du sulfate de sodium Na2SO4) est mis en solution dans l'eau afin de la rendre plus conductrice. On branche une source de tension continue entre les deux électrodes, de façon à maintenir une différence de potentiel constante entre elles. Le processus d’électrolyse (séparation à l’aide d’un courant électrique) de l’eau commence. 1) A l’électrode négative (cathode) :- Spoiler:
| (A)
Les ions positifs (ici Na+) sont attirés vers l’électrode négative
(celle-ci est couverte d’un surplus d’électrons "poussés" là par
la source de tension).
Chaque ion est entouré d’un cortège de molécules d’eau.
| | (B)
Le côté positif (atomes d’hydrogène) des molécules d’eau est
fortement attiré par l’électrode négative. Certaines des
molécules d’eau se séparent en un ion H+ et un ion OH-. L’ion
positif et les ions OH- qui l’entourent sont, globalement, négatifs
et sont repoussés par l’électrode négative.
Les ions H+ se combinent avec des électrons de l’électrode
et deviennent des atomes d’hydrogène (H). | | (C)
Les atomes d’hydrogène se groupent par paires et s’en vont
vers la surface de l’eau sous forme de molécules
d’hydrogène (H2). Les bulles de gaz visibles à l’œil nu sont
formées de millions de molécules d’H2. Quatre électrons
provenant de la source viennent remplacer les quatre
électrons utilisés pour former deux molécules de H2. |
2) A l’électrode positive (anode) :- Spoiler:
| (A)
Les ions négatifs (ici SO4) sont attirés vers l’électrode
positive (celle-ci manque d’électrons qui ont été "poussés"
vers l’électrode négative par la source de tension).
Chaque ion est entouré d’un cortège de molécules d’eau.
| | (B)
Le côté négatif (atomes d’oxygène) des molécules d’eau
est fortement attiré par l’électrode positive. Certaines des
molécules d’eau se séparent en un ion O2- et 2 ions H+.
L’ion négatif et les ions H+ qui l’entourent sont, globalement,
positifs et sont repoussés par l’électrode positive. Les deux
électrons en trop de chaque ion O2- se font arracher par
l’électrode positive et les ions O2-deviennent des atomes
d’oxygène (O). | | (C)
Les atomes d’oxygène se groupent par paires et s’en vont vers
la surface de l’eau sous forme de molécules d’oxygène (O2).
Les quatre électrons captés par l’électrode positive sont attirés
vers la source de tension. Les ions H+ restés autour des ions
négatifs vont éventuellement se combiner avec des ions OH-
restés autour des ions positifs pour former des molécules d’eau. |
Sans vouloir occulter l'électrode positive, c'est quand même du côté de l'électrode de l'hydrogène que notre attention va quand même se porter.@++ | |
|   | | Asl
Support Electronique
Membre d'Honneur


Age : 73
Localisation : Près de Saumur
Prénom : Alain
Date d'inscription : 15/08/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mer 3 Déc 2008 - 21:10 Mer 3 Déc 2008 - 21:10 | |
| Bonjour, Je me permets de reformuler l'explication à ma manière afin de marquer certains points qui me paraissent importants. Et bien sûr, surtout me corriger si je fais fausse route dans mon explication.Quatre phases donc : 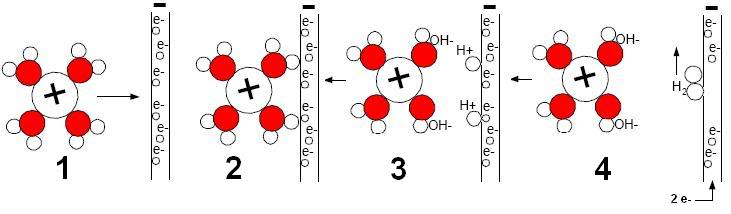 - L'ion de Na+(accompagné par une "nuée" de molécules d'eau) est attiré par l'électrode.
Cette électrode, du fait du courant existant, possède des électrons libres (-) à sa surface.
- L'ion Na+ touche, ou du moins se rapproche suffisant près de l'électrode.
- A ce moment cette attirance est plus forte que l'équilibre "ion Na+ et molécules" ce qui provoque une rupture des liaisons existantes : le noyau de l'atome d'hydrogène se sépare pour "rejoindre" l'électrode.
Mais uniquement le noyau (+) car son électron (-) est plutôt repoussé (au fait, que devient-il ?). Ce noyau devient donc un ion H+ (c'est un atome qui a perdu son électron).
Et l’ion positif (Na+) et les ions OH- qui l’entourent étant globalement négatifs sont repoussés par l’électrode négative.
- Chaque ion H+ prélève un électron (-) sur l'électrode et (re)devient un atome d'hydrogène.
Et deux atomes d'hydrogène se combinent pour former une molécule d'hydrogène.
Et la quantité forme.... des bulles ! 
Si tout est juste, il y a une question subsidiaire (et la réponse est peut-être importante pour nous) : A la phase 1, Les ions positifs (Na+) "amènent" les molécules d'eau à l'électrode.
Et c'est là que j'ai du mal à comprendre.
Car même sans électrolyte (sulfate de sodium), de toute façon les molécules d'eau sont déjà en contact permanent avec l'électrode.
Donc pourquoi n'y a-t-il pas ruptures des liaisons de la molécule d'eau comme dans (3) ?
Qu'est-ce que l'ion Na+ apporte en plus ?
Rapprocher les molécules d'eau ? Mais elles sont déjà en contact avec l'électrode !! @++ PS : Pour correction ou explication, grand merci d'utiliser un autre style que celui-ci par exemple :
AlCl3 + PCl2 => MgBr2 + Na4 -OH 6
Merci d'avance. | |
|   | | fc89
Chef de projet
Membre Donateur


Age : 60
Localisation : Bourgogne, France
Prénom : Francis
Date d'inscription : 07/11/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mer 3 Déc 2008 - 21:35 Mer 3 Déc 2008 - 21:35 | |
| Bonsoir Alain,
Dans tout ça, comme notre eau n'est pas pure, il y certainement le phénomène oxydo-réduction.
Un sacré nom barbare, qui tente de libérer un surplus d' électrons positifs ou négatifs selon le composant chimique dans l'eau (pollution ou additif dans l'eau) par oxydation de ce composant.
Avec de l'eau pure à 100%, je pense qu'il ne se passerais rien!
Mais l'eau n'est pas pure, il y a donc oxydo-réduction.
Certain métaux, avec de l'eau et du courant, font également de l'oxydo-réduction.
Mais comme je ne suis pas chimiste, je ne pourrai étayer tout ça!
A+ | |
|   | | JCV
Support Electronique
Age : 75
Localisation : France (Nord)
Prénom : Jean-Claude
Date d'inscription : 28/04/2008
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Jeu 4 Déc 2008 - 12:52 Jeu 4 Déc 2008 - 12:52 | |
| Bonjour,
Je pense aussi, comme le dit Francis, que:
Si on prend une eau parfaitement pure, ne contenant pas d'ions, des électrodes parfaitement propre qui n'interréagissent pas avec l'eau. Il n'y aura aucun échange et aucune production d'hydrogéne et oxygène. Il n'y a pas de courant et cette eau est un parfait isolant.
Il faut absolument qu'il y ait des ions pour provoquer cette électrolyse.
Donc, pour produire une électrolyse, il nous faut deux choses :
- Des ions.
- Un contact d'échange d'électrons (les électrodes).
Fabriquer des ions: classiquement, on utilise un sel. Mais on peut imaginer d'autres moyens, parmis ceux déjà vu il y a: champ électrique par haute tension, arc électrique, champ magnétique, micro-ondes, lumière (laser), et d'autres que j'ai oublié.
Echange d'électrons: classiquement, les électrodes. On prends deux électrons sur la cathode pour faire une molécule d'hydrogéne, et on restitue deux électrons sur l'anode pour faire un atome d'oxygène. Mais serait-il possible que les ions puissent faire cet échange sans passer par un support extérieur ? .
A+
JCV | |
|   | | Asl
Support Electronique
Membre d'Honneur


Age : 73
Localisation : Près de Saumur
Prénom : Alain
Date d'inscription : 15/08/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Jeu 4 Déc 2008 - 14:44 Jeu 4 Déc 2008 - 14:44 | |
| Bonjour, Oui, c'est aussi ce que je pense. C'est pour cette raison qu'il nous faut trouver la réponse à : - Citation :
- Qu'est-ce que l'ion Na+ apporte en plus ?
Par nous-mêmes ou avec l'aide d'un chimiste compétent et surtout ouvert d'esprit. Car depuis que je connais un peu plus dans le détail le fonctionnement de l'électrolyse, je m'aperçois qu'en réalité il ne faut vraiment pas grand'chose pour séparer l'atome d'hydrogène. Vraiment très très peu d'énergie.Mais uniquement lorsque l'atome se trouve dans un contexte bien particulier. C'est pour cette raison que je continue sur cette voie, d'abord essayer de comprendre les différents mécanismes chimiques à ce sujet pour pouvoir, je l'espère, en retirer et adapter la ou les clés qui pourront être implantés sur notre futur système. Mais... commencer impérativement par le début. Nous voulons commander l'atome d'hydrogène ? Commençons donc par le connaitre, savoir au moins comment il vit, il réagit. Après, si solution trouvée, ce ne sera qu'une toute bête mise en application. @++ | |
|   | | Asl
Support Electronique
Membre d'Honneur


Age : 73
Localisation : Près de Saumur
Prénom : Alain
Date d'inscription : 15/08/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Dim 7 Déc 2008 - 10:46 Dim 7 Déc 2008 - 10:46 | |
| Bonjour, J'effectue, comme vous des recherches à ce sujet, mais je voudrais préciser que trouver des articles chimiesques qui présentent à longueur de lignes des hiéroglyphes du style : - Citation :
4H2O + 4 e- => 2H2 + 4 OH-
et
2H2O => O2 + 4 H+ + 4 e-
Donc : 2H2O => 2H2 + O2 n'offre strictement aucun intérêt ! Pour info, il semblerait que ce soient les formules "expliquant" l'électrolyse !!!Or, ce n'est pas avec cette ou ces formules que l'on va pouvoir effectuer une quelconque mise en application pour nous. J'en reviens à mon 2ème message du sujet qui comporte quelques questions (il y en d'autres en attente) et qui doivent trouver leurs réponses. Mais ces réponses ne se trouvent pas dans une formule. Car une formule n'est que la preuve, la vérification, du résultat du phénomène produit et non son explication. Donc si vous trouvez un site qui pourrait permettre de nous aider dans ce sens... Ou mieux, si vous connaissez un chimiste capable, non pas d'énoncer les formules résultants d'une réaction, mais d'expliquer cette réaction (en disant, par exemple : " ... à ce moment, l'atome étant soumis au champ électrique, se sépare de la molécule et va...etc...)"... Nous vous lirons avec grand plaisir ! @++ | |
|   | | iaorana
Membre Super Actif

Age : 82
Localisation : Polynésie Française
Prénom : Alain
Date d'inscription : 01/12/2008
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Lun 8 Déc 2008 - 21:31 Lun 8 Déc 2008 - 21:31 | |
| Ia ora na à tous, On est ici dans un sujet électrolyse de l'eau au sens strict, n'est-ce-pas ? A l'attention de ceux qui "débarquent", puis-je néanmoins rappeler ceci : Les divers procédés pour extraire de l'hydrogène de l'eau ne sont pas tous à base d'électrolyse - loin s'en faut - notamment la cellule dite de Meyer où, sauf fuites parasites, il n'y a aucun transfert d'électrons entre les armatures de la cellule (considérée comme un condensateur) et le liquide, et que dans ce cas la présence d'ions dans l'eau n'est pas nécessaire. On y soumet l'eau (pure ou pas) à un champ électrique variable censé "craquer" les molécules d'eau...  - Voir rubrique Meyer. Alain | |
|   | | iaorana
Membre Super Actif

Age : 82
Localisation : Polynésie Française
Prénom : Alain
Date d'inscription : 01/12/2008
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mar 9 Déc 2008 - 2:07 Mar 9 Déc 2008 - 2:07 | |
| - Asl a écrit:
- si vous connaissez un chimiste capable, non pas d'énoncer les formules résultants d'une réaction, mais d'expliquer cette réaction (en disant, par exemple : "... à ce moment, l'atome étant soumis au champ électrique, se sépare de la molécule et va...etc...)"...
C'est ce qui, voici euh... 48 ans, m'a fait prendre la Chimie organique en grippe. Mais depuis, la connaissance (interprétation) physique a dû progresser, je suppose... Alain | |
|   | | Asl
Support Electronique
Membre d'Honneur


Age : 73
Localisation : Près de Saumur
Prénom : Alain
Date d'inscription : 15/08/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mar 9 Déc 2008 - 2:30 Mar 9 Déc 2008 - 2:30 | |
| Bonsoir, Tout à fait exact. Et pour tous ceux qui "débarquent", je rappelle qu'il n'est pas question dans ce sujet de réaliser une électrolyse (d'ailleurs pour cela vous n'aurez besoin ni du Forum ni de personne). Car je me suis aperçu que très peu de monde (oserai-je dire personne ?) ne connait l'électrolyse dans ses moindres détails (et moi le premier). Donc ce sujet n'est qu'une base de recherche tout d'abord, puis de discussions. Je pense que si nous connaissons dans le détail, le contexte dans lequel notre petit atome d'hydrogène se sépare de celui d'oxygène, pourrons-nous avoir l'idée, peut-être, de recréer un élément de ce contexte, sur notre système, qui permettrait de provoquer cette séparation. Peut-être pas mais... peut-être que oui. Dans tous les cas, ça vaut la peine d'être tenté. Et depuis que j'avance sur ce sujet, je me suis aperçu qu'il fallait très peu, mais vraiment très peu d'énergie, pour séparer ces 2 atomes, contrairement à tout ce qui a pu être dit jusque là. Un peu exagéré ? Que nenni ! Pensez, une toute petite pile de 1,5v... et j'en retire de l'hydrogène ET de l'oxygène. Il nous faut en connaitre tous les éléments du contexte et voir si on peut le(s) transposer dans le notre. @++ PS : Alain, tu as posté ton message pendant que j'écrivais :
- Citation :
- ...m'a fait prendre la Chimie organique en grippe...
Alors je ne sais pas si tu as été un jour mon prof, mais là, je peux t'assurer que nous avons du avoir le même prof de chimie !!!  | |
|   | | JCV
Support Electronique

Age : 75
Localisation : France (Nord)
Prénom : Jean-Claude
Date d'inscription : 28/04/2008
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mar 9 Déc 2008 - 19:05 Mar 9 Déc 2008 - 19:05 | |
| Bonjour,
Dans le calcul suivant nous allons d'abord essayer de déterminer la quantité de gaz maximum que peut produire 1g d'eau. Avec ce gramme, on ne pourra jamais produire plus que le résultat de ce calcul.
Puis nous allons déterminer quelle est la production de gaz maximum en fonction du courant. Bon, ici c'est de l'electrolyse classique, mais faute de mieux pour l'instant.
Tous les calculs se feront par simple comptage d'atomes, molécules, électrons.
Sauf erreur ou mauvaise interprétation de ma part:
Rappels:
- Notation : 10^23 = 10 puissance 23
- Nombre d'Avogadro : donne le nombre de molécules ou d'atomes par moles : Na = 6.022 x 10^23
- La masse atomique est la masse d'une mole d'atomes.
- Volume d'une mole de gaz à la température de 20°C et à la pression de 1013 hPa = 22.4 L
- Charge élémentaire de l'électron : -e = 1.602 x 10^-19 coulombs
1 - Calcul de la quantité de gaz que peut fournir 1g d'eau
- L'hydrogène à une masse atomique de 1g / mole
- L'oxygène à une masse atomique de 16g / mole
Comme l'eau est constituée de 2 atomes d'hydrogène et de 1 atome d'oxygène, elle a une masse atomique de 1 + 1 + 16 = 18g / mole
Comme on sait que une mole d'eau contient Na molécules, et pèse 18g, on peut en déduire le nombre de molécules dans 1g d'eau:
- un gramme d'eau va contenir : 6.022 x 10^23 / 18 = 33.4556 x 10^21 molécules
Et comme chaque molécule d'eau contient 2 atomes d'hydrogène et 1 atome d'oxygène, on peut déduire que 1g d'eau contient :
33.4556 x 10^21 atomes d'oxygène.
66.9111 x 10^21 atomes d'hydrogène.
Si par un procédé quelconque (électrolyse par exemple) on sépare ce gramme d'eau en ses constituants élémentaires, on obtiendra au maximum (note: il faut deux atomes pour faire une molécule d'oxygène ou d'hydrogène):
16.7278 x 10^21 molécules d'oxygène.
33.4556 x 10^21 molécules d'hydrogène.
On sait que quelque-soit le type de gaz, à la température ambiante et à pression normale, une mole (6.022 x 10^23 molécules) de gaz occupe un volume de 22.4 litres.
On peut donc calculer le volume de gaz occupé :
L'oxygène va occuper : 22.4 x 16.7278 x 10^21 / 6.022 x 10^23 = 0.622 litres.
L'hydrogène va occuper : 22.4 x 33.4556 x 10^21 / 6.022 x 10^23 = 1.244 litres.
Si les deux gaz sont mélangés, ils occupent 0.622 + 1.244 = 1.866 litres de gaz HHO.
1 gramme d'eau donne au maximum 1.866 litres de HHO
HHO : gaz oxyhydrogène
(Rappel: 1g d'eau = 1 milli-litre)
Donc 1 litre d'eau (soit 1 kg) donnera 1866 litres de gaz HHO.
On peut comprendre facilement que lors d'une électrolyse forte, le dégagement gaseux peut être impréssionant.
2 - Electrolyse, détermination de la production de gaz en fonction du courant
On sait que 1 ampère = 1 coulomb par seconde.
On calcule le nombre d'électrons correspondant à 1 coulomb, comme la charge de l'électron est de 1.602 / 10^19 coulombs, il y a donc :
1 / 1.602 / 10^19 = 6.24 x 10^18 électrons dans 1 coulomb.
Dans la description d'Alain ci-dessus, on voit qu'il faut 4 électrons pour produire 1 molécule d'oxygène et 2 molécules d'hydrogène.
Donc 1 coulomb par seconde (= 1 ampère) va produire :
1 x 6.24 x 10^18 / 4 = 1.56 x 10^18 molécules d'oxygène
2 x 6.24 x 10^18 / 4 = 3.12 x 10^18 molécules d'hydrogène
Soit un volume par ampère et par seconde de :
22.4 x 1.56 x 10^18 / 6.022 x 10^23 = 58 x 10^-6 litres d'oxygène
22.4 x 3.12 x 10^18 / 6.022 x 10^23 = 116 x 10^-6 litres d'hydrogène
Pour connaître le volume par ampère pour une heure on multiplie par 3600 :
Soit:
Oxygène : 58 x 10^-6 x 3600 = 0.209 Lh/A
Hydrogène : 116 x 10^-6 x 3600 = 0.418 Lh/A
Si les deux gaz sont mélangés, la production est de 0.209 + 0.418 = 0.627 Lh/A de gaz HHO.
La production de gaz HHO est de 0.627 Lh/A (litres.heure par ampère)
Ce calcul un peu compliqué nous permet de retrouver ce qui peut être obtenu plus simplement en appliquant la loi de Faraday.
Remarque: dans une électrolyse, la quantité de gaz produite par unité de temps est proportionnelle au courant, et indépendante de la tension, on a donc interet à fonctionner avec une tension la plus faible possible, mais on sera limité par l'effet de pile et la résistivité de l'eau.
La tension d'effet de pile dépend des électrodes (matière, état de surface, traitement, ... )
La résistivité dépend principalement du taux d'ionisation de l'eau.
A+
JCV | |
|   | | fc89
Chef de projet
Membre Donateur


Age : 60
Localisation : Bourgogne, France
Prénom : Francis
Date d'inscription : 07/11/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mar 9 Déc 2008 - 19:35 Mar 9 Déc 2008 - 19:35 | |
| Bonjour Jean-Claude, Très bel exposé que tu nous fais, là! Comme cela messieurs, vous savez ce que donne une électrolyse classique. - Citation :
- La production de gaz HHO est de 0.627 Lh/A (litres.heure par ampère)
Il faut absolument prendre ce résultat comme moyen de comparaison. A+ | |
|   | | Asl
Support Electronique
Membre d'Honneur


Age : 73
Localisation : Près de Saumur
Prénom : Alain
Date d'inscription : 15/08/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mar 9 Déc 2008 - 20:04 Mar 9 Déc 2008 - 20:04 | |
| Bonjour, En effet, exposé très clair, précis et surtout compréhensible par tous (même par moi, c'est tout dire !!). - Citation :
- Volume d'une mole de gaz à la température de 20°C et à la pression de 1013 hPa = 22.4 L
Est-ce si sûr ? Car il me semble que quelque soit la pression/température, tout gaz occupe entièrement toujours le volume de son contenant, quelque soit son volume. Heureusement d'ailleurs sinon, on aurait créé "le vide". Mais je ne suis pas sûr que cette remarque influe d'une quelconque façon sur les calculs suivants. @++ | |
|   | | JCV
Support Electronique

Age : 75
Localisation : France (Nord)
Prénom : Jean-Claude
Date d'inscription : 28/04/2008
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mar 9 Déc 2008 - 20:42 Mar 9 Déc 2008 - 20:42 | |
| Re, En principe, j'essaye toujours d'être clair et precis, ce n'est pas toujours évident, mais ça fait palisir de l'entendre dire. - Asl a écrit:
-
- Citation :
- Volume d'une mole de gaz à la température de 20°C et à la pression de 1013 hPa = 22.4 L
Est-ce si sûr ?
Car il me semble que quelque soit la pression/température, tout gaz occupe entièrement toujours le volume de son contenant, quelque soit son volume.
Heureusement d'ailleurs sinon, on aurait créé "le vide".
Mais je ne suis pas sûr que cette remarque influe d'une quelconque façon sur les calculs suivants. Il me semble que c'est lié à la formule P.V = nR.T (Pression x Volume = constante x Température). Voir: http://fr.wikipedia.org/wiki/Volume_molaire A+ JCV | |
|   | | tom
Chef de Projet

Age : 54
Localisation : somme 80
Prénom : Tom
Date d'inscription : 10/12/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mar 9 Déc 2008 - 21:13 Mar 9 Déc 2008 - 21:13 | |
| Génial JC!
Moi je dis qu'il faut garder nos anciens absolument, car nous autres (surtout moi!) avons un grand besoin de leurs savoir!
Avec toutes ces recherches, on va pouvoir y arriver tot ou tard! ;) | |
|   | | Asl
Support Electronique
Membre d'Honneur


Age : 73
Localisation : Près de Saumur
Prénom : Alain
Date d'inscription : 15/08/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mar 9 Déc 2008 - 21:24 Mar 9 Déc 2008 - 21:24 | |
| Bonsoir, Je me joins totalement à Tom pour dire : IL FAUT GARDER A TOUT PRIX NOS ANCIENS !! Alors, Jean-Claude, Heureux ?  Restons sérieux !!!! Merci de la précision, car en effet il s'agit de "volume molaire" (tiens, j'ai encore appris quelque chose ! Il est vraiment extra ce Forum !!!). Une unité en quelque sorte pour pouvoir justement définir l'espace occupé par un gaz. Unité donc valable pour tous les gaz. Merci Jean-Claude. Ouf ! Je suis fatigué... je retourne à l'école... @++ | |
|   | | iaorana
Membre Super Actif

Age : 82
Localisation : Polynésie Française
Prénom : Alain
Date d'inscription : 01/12/2008
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Mar 9 Déc 2008 - 22:10 Mar 9 Déc 2008 - 22:10 | |
| - Asl a écrit:
- Ouf ! Je suis fatigué... je retourne à l'école...
Boyle-Mariotte, c'est pas mariole  Tous à vos gadrots !  OK, je sors...;) | |
|   | | tophe71
Membre d'Honneur

Age : 59
Localisation : France
Prénom : Christophe
Date d'inscription : 23/08/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Jeu 11 Déc 2008 - 9:04 Jeu 11 Déc 2008 - 9:04 | |
| Bonjour, - Citation :
- La production de gaz HHO est de 0.627 Lh/A (litres.heure par ampère)
C'est quand même pas une nouveauté, depuis le début de mes essais et notamment en réel sur ma Clio, c'est cette formule qui m'a permis de vérifier mon rendement d'électrolyse. A+ | |
|   | | iaorana
Membre Super Actif

Age : 82
Localisation : Polynésie Française
Prénom : Alain
Date d'inscription : 01/12/2008
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Jeu 11 Déc 2008 - 10:25 Jeu 11 Déc 2008 - 10:25 | |
| - tophe71 a écrit:
- C'est quand même pas une nouveauté, depuis le début de mes essais et notamment en réel sur ma Clio, c'est cette formule qui m'a permis de vérifier mon rendement d'électrolyse.
OK, mais JCV l'explique et le démontre magistralement - ça ne fait pas de mal de se rafraîchir les cellules mémoires ;). Merci Jean-Claude  | |
|   | | JCV
Support Electronique

Age : 75
Localisation : France (Nord)
Prénom : Jean-Claude
Date d'inscription : 28/04/2008
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Jeu 11 Déc 2008 - 20:00 Jeu 11 Déc 2008 - 20:00 | |
| Bonsoir Christophe,
Je sais bien que ce n'est pas une nouveauté, mais je voulais retrouver par calcul ce que tout le monde écrit comme ci c'était évident. Je suis électronicien, et ne connais plus grand chose en chimie (cela remonte à trop loin).
Le but était aussi de trouver combien de litre d'oxygène et d'hydrogène on peut extraire d'un gramme d'eau (déduire pour un litre). Valeur qu'il est impossible de dépasser quelque soit le procédé de craquage des molécules d'eau.
On voit aussi qu'avec une électrolyse classique on peut complètement transformer l'eau en gaz, cela dépend juste du temps et du courant. Il n'y a pas de superproduction possible.
Et cela indique aussi qu'il faut trouver une autre méthode (non chimique de préférence) pour "craquer" les molécules d'eau en utilisant le moins possible d'énergie, et en poluant le moins possible.
Amicalemnt
JCV | |
|   | | miri
Membre Actif
Age : 58
Localisation : polynesie francaise
Prénom : herve
Date d'inscription : 01/12/2008
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Ven 4 Sep 2009 - 5:05 Ven 4 Sep 2009 - 5:05 | |
| Ia ora na
Donc, pour revenir au debut du topic, pour avoir un H monoatomique, il ne faut pas qu'un électron de l'electrode puisse passer dans l'eau?
Pourrait on imaginer une electrolyte suivante: ion+ d'un coté (O) et ion- de l'autre (H), qui permettrait un desequilibre electrique (+,-) superieur ?
Sur ton shema, Alain, il n'ya qu'une molecule: quid des liaisons hydrogene?
Ds l'exemple, l'electrolyse est Na+SO4-.Que se passe t il si on mettait que du Na+.
Voila pleins de questions betes alors, si vs avez les reponses.......
Merci de votre tolerance
Rv | |
|   | | Asl
Support Electronique
Membre d'Honneur


Age : 73
Localisation : Près de Saumur
Prénom : Alain
Date d'inscription : 15/08/2006
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  Ven 4 Sep 2009 - 13:35 Ven 4 Sep 2009 - 13:35 | |
| Bonjour Hervé, Je suis assez content que le sujet reprenne car je reste persuadé que si nous avons une vison précise de ce qui ce passe exactement au niveau moléculaire, et de toutes les "forces" qui agissent pour l'électrolyse, nous pourrons probablement trouver une des clés indispensables à nos recherches.Mais mon niveau de chimie est quasi nul... - Citation :
- Donc, pour revenir au debut du topic, pour avoir un H monoatomique, il ne faut pas qu'un électron de l'electrode puisse passer dans l'eau?
Oui, c'est le système du type Eccles ou du moins avec les électrodes isolées (d'ailleurs que se passerait-il s'il n'y en avait qu'une seule, celle qui nous intéresse, d'isolée ?). Mais probablement, pour qu'il y ait des "bulles", faut-il une molécule (dy-hydrogène dans ce cas) et non deux petits atomes d'hydrogène qui se baladent tout seul. - Citation :
- Sur ton shema, Alain, il n'ya qu'une molecule: quid des liaisons hydrogene?
Tous les schémas sont des schémas que j'ai repris sur le net (avec leurs explications). Je l'ai ai légèrement modifiés pour transcrire d'une façon plus compréhensible ce que j'avais compris (en espérant ne pas mettre trompé).Et donc, toujours et uniquement d'après ce que j'ai compris, les liaisons hydrogène existent... avec l'électrolyte. - Citation :
- Ds l'exemple, l'electrolyse est Na+SO4-.Que se passe t il si on mettait que du Na+.
Excellente question... Mais impossible pour moi d'y répondre. Et des questions (ou plutôt leurs réponses) sont nombreuses. Dans mon topic, je posais une question similaire à la tienne : - Moi-même a écrit:
- Car même sans électrolyte (sulfate de sodium), de toute façon les molécules d'eau sont déjà en contact permanent avec l'électrode. Donc pourquoi n'y a-t-il pas ruptures des liaisons de la molécule d'eau comme dans (3) ?
Je m'étais inscrit sur deux forums de chimie en espérant trouver quelques réponses. Mais ce n'est pas facile. Il y a des "têtes" en chimie mais en trouver un qui réponde de façon simple et logique est assez difficile. En général le type de réponse est du style : " AlCl3 + PCl2 => MgBr2 + Na4 -OH 6" !! Et pour m'aider à décoder ça... j'ai besoin de l'aide de Champollion !  @++ | |
|   | | Contenu sponsorisé
 |  Sujet: Re: L'électrolyse, mais c'est très simple... Sujet: Re: L'électrolyse, mais c'est très simple...  | |
| |
|   | | | | L'électrolyse, mais c'est très simple... |  |
|
Sujets similaires |  |
|
| | Permission de ce forum: | Vous ne pouvez pas répondre aux sujets dans ce forum
| |
| |
| | Bonjour, vous êtes le |
ème visiteur
Et nous sommes le
|
| Quelle langue ? |
Translate entire Forum in your language
Traducir toda Foro en su idioma
Tradurre tutto il Forum nella tua lingua
Traduzir Fórum inteira no seu idioma
Перевести весь форум на вашем языке
|
VOUS VOULEZ NOUS REFERENCER
SUR VOTRE SITE, BLOG OU FORUM ? |
Comment faire...
Copier le code ci-dessous :
| Code: | <a href="http://generation-hydrogene.forumpro.fr/" target="_blank"><img src="http://i29.photobucket.com/albums/c280/SAlain/Forum/Logos/GH_Petit.gif" alt="Génération Hydrogène" width="250" height="70" /></a> |
Collez-le sur votre page...
La bannière suivante s'affichera :
Et Merci d'avance...
Pensez à m'en informer par MP...
(Admin)
|
| Pensez à soutenir nos projets... |  Ne jamais commencer un projet sans avoir toutes les ressources nécessaires |
| Site à visiter... |

|
NOS REALISATIONS, TESTEES ET...
REPRODUCTIBLES PAR TOUS ! |
Alimentation à découpage
2v - 25v / 20A |
|
|
Carte interface série optocouplée
pour système de développement
sur PICS |
|
|
Carte PWM avec
mosfet de puissance intégré |
|
|
|
|

